Arrojan pistas para el tratamiento de un agresivo tumor pediátrico
Científicos del Hospital Garrahan, del Instituto Leloir, del CONICET y colegas descubrieron mecanismos moleculares que explicarían por qué en algunos casos falla la respuesta de un subtipo de tumor ocular a la quimioterapia. También identificaron fármacos con capacidad terapéutica.
Un estudio internacional liderado por investigadores del Hospital Garrahan, de la Fundación Instituto Leloir (FIL) y del CONICET logró identificar factores genéticos que explicarían por qué un tumor pediátrico es resistente a la acción de la quimioterapia. Y también identificaron en un modelo animal fármacos que tendrían la capacidad de derrotarlo.
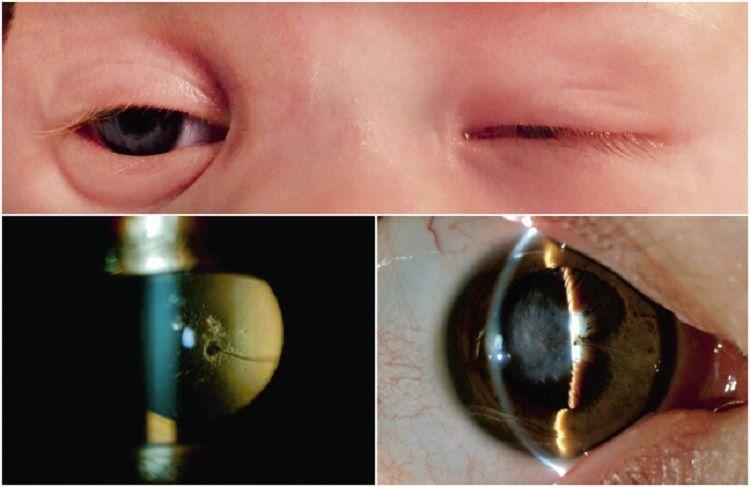
El retinoblastoma, un tipo de tumor ocular en niños, se puede eliminar cuando se detecta en forma temprana y suele ser sensible a la quimioterapia. Sin embargo, el pronóstico empeora si el cáncer se disemina principalmente al sistema nervioso central: en esos casos, hasta 9 de cada 10 pacientes no logra curarse pese a la quimioterapia, los rayos y la cirugía.
El nuevo estudio, liderado por científicos argentinos y en colaboración con médicos de India y de Estados Unidos e investigadores de Francia y España, se centró en un subtipo de retinoblastoma agresivo que corresponde al 2% de los casos y que hasta el momento carece de tratamiento adecuado.
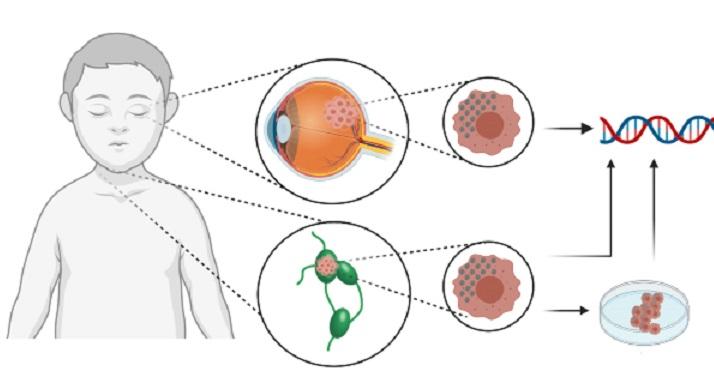
Con el consentimiento de los padres, los investigadores obtuvieron material del tumor primario y sitios metastásicos de retinoblastomas refractarios a quimioterapia de dos niños de 17 y de 30 meses de edad. Y realizaron estudios genómicos que permitieron identificar una curiosa serie de alteraciones genéticas que explicarían la resistencia de ese tipo de cáncer al tratamiento convencional. El trabajo fue publicado en la revista de acceso abierto
Cancers.
«Llamativamente, los tumores no mostraron mutaciones en el gen RB1, característico de retinoblastoma, pero si alteraciones del gen MYCN, combinación reportada en solo el 2% de los casos de este tumor», afirmó Andrea Llera, una de las líderes del estudio y directora de la Unidad asociada de Genómica en Cáncer ´Genocan´, que funciona en la FIL.
Los científicos también identificaron una inesperada mutación en TP53, gen que ´como si fuera un dogma´ se consideraba inalterado en retinoblastoma, agregó una primera autora del estudio, la bioinformática Daiana Ganiewich, becaria doctoral de la Fundación Leo Messi que trabaja bajo la codirección de Llera en el Garrahan. También se descubrieron alteraciones en los cromosomas 16q y 17p.
Paula Schaiquevich (izq.) Andrea Llera, directoras del estudio, y Daiana Ganiewich y Santiago Zugbi, primeros autores.
Los estudios genómicos se realizaron en colaboración entre investigadores de la FIL, del Hospital Curie (Paris, Francia) y del Hospital Sant Joan de Deu (Barcelona, España).
La búsqueda de medicamentos
En una segunda fase de la investigación, los científicos establecieron modelos celulares (in vitro) de ese retinoblastoma agresivo en el Hospital Garrahan y modelos animales (in vivo) de esa enfermedad en la FIL. Y realizaron en ellos un análisis farmacológico en colaboración con el Memorial Sloan Kettering Cancer Center, en Nueva York (Estados Unidos) y con el apoyo de una beca de la Fundación Bunge y Born.
«Estos estudios permitieron identificar 17 fármacos como posibles candidatos por su actividad para tratar estas células tumorale», explicó otro primer autor, el bioquímico y farmacéutico Santiago Zugbi, becario doctoral del CONICET en el Garrahan.
Luego, los investigadores seleccionaron un grupo reducido de esos fármacos que, por su disponibilidad en el mercado y características farmacológicas, podrían sugerir efectividad in vivo y factibilidad de traslación a la clínica. «Estas combinaciones novedosas fueron evaluadas en modelos celulares y animales y demostraron mayor actividad antitumoral que el tratamiento convencional», destacó Paula Schaiquevich, también líder del estudio, una investigadora del CONICET que dirige la Unidad de Tratamientos Innovadores del Garrahan.
«De ese grupo de fármacos, panobinostat, bortezomib y carboplatino demostraron actividad sinérgica in vitro y sería factible su indicación en este subtipo de retinoblastoma», indicó Schaiquevich. Ensayos clínicos o protocolos de uso compasivo podrían ayudar a confirmar esa hipótesis.
«Dada la evidencia de ciertos marcadores genómicos que nos indican la agresividad del tumor, estos pacientes deberían ser identificados para no recibir tratamientos convencionales que se sabe que no van a ser efectivos», puntualizó Llera, para quien hay que tomar decisiones terapéuticas acordes al cuadro clínico.
Llera también destacó que «el estudio es la primera descripción de un tumor de estas características moleculares, y hasta ahora la primera y única evaluación farmacológica del mismo basada en modelos animales usando muestras de pacientes y que en la jerga científica se llaman ´modelos PDX o CDX´ que son lo último en medicina traslacional».
Del estudio también participaron Osvaldo Podhjacer y Eduardo Cafferata, de la FIL y del CONICET; Guillermo Chantada, Rosario Aschero, Mariana Sgroi, Claudia Sampor, Fabiana Lubieniecki. Gabriela Lamas, Ursula Winter, Marcela Mena, Manuel Daroqui, Edgardo Baialardo y Adriana Fandiño, del Hospital Garrahan (los primeros dos, también del CONICET); François Radvanyi y Daniela Ottaviani, del Institut Curie, Paris; Mariona Suñol y Cinzia Lavarino, del Hospital Sant Joan de Deu, en Barcelona, España; Arpita Bhattacharyya y Anirban Das, del Tata Memorial Hospital, Calcuta, India; Beatriz Salas, del Hospital Asencio Villaroel, Cochabamba, Bolivia, y Jasmine Francis, David Abramson y Ralph Garippa, del Memorial Sloan Kettering de Nueva York, Estados Unidos.
El estudio contó con el apoyo de varios organismos y fundaciones de Argentina: la Agencia Nacional de Promoción de la Investigación, el Desarrollo Tecnológico y la Innovación, el Instituto Nacional del Cáncer, la Fundación Natali Dafne Flexer, la Fundación Garrahan y el Instituto Henry Moore.
También aportaron fondos la Fundación Leo Messi, con sede en Barcelona; la Fondation Nelia et Amadeo Barletta, con base en Suiza; y Fund for Ophthalmic Knowledge, Amazon Web Services Cloud Credits for Research y los Institutos Nacionales de Salud (NIH) de Estados Unidos.
Ref: Agencia CyTA-Leloir


 Por buenapraxis
Por buenapraxis